细品教材
在化学变化中,原子不能再分,也就是说原子不能再破裂,它是化学变化中的最小粒子。1897年,英国科学家汤姆生发现电子,证明原子的可分性。1911年,卢瑟福的α粒子散射实验,更明确地证明了原子是可分的。

一、原子核外电子的排布
1.原子结构模型

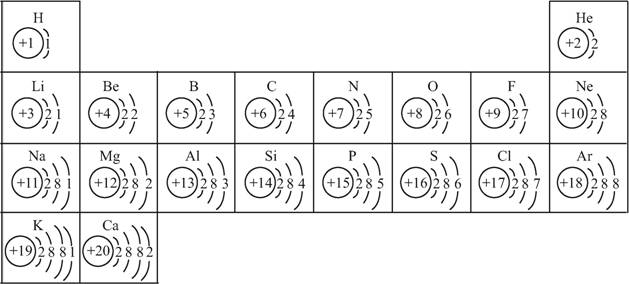
1~20的原子结构示意图
2.电子层的划分
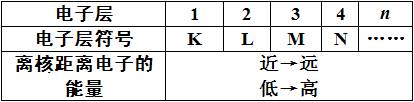
人们把核外电子运动的不同区域看成不同的电子层,各电子层由内向外的序数n依次为1、2、3、4、5、6、7……分别称为K、L、M、N、O、P、Q……电子层。其中离核近的电子层中运动的电子能量较低,离核远的电子层中运动的电子能量较高。例如:钠原子核外有11个电子,它们分三层排布,分别处于核外K、L、M电子层中,最外层M层的1个电子能量最高。
3.核外电子的排布规律
核外电子的排布规律是:
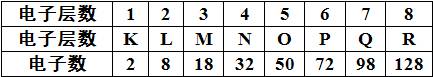
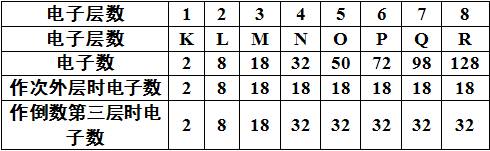
(1)各层最多能容纳的电子数是2n2(n表示电子层序数)。
状元笔记:
在含有多个电子的原子里,电子依能量不同分层排布,能量低的电子通常在离核较近的区域内运动,能量高的电子通常在离核较远的区域内运动,离核越近的电子层能量越低。
(2)各原子最外电子层上能容纳的电子数不超过8个(K层为最外层时不超过2个电子)。
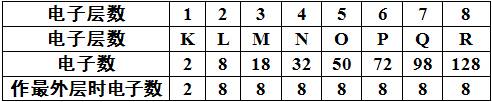
(3)次外电子层上不超过18个电子,倒数第三层上最多不超过32个电子。
(4)核外电子总是尽可能先排在能量最低的电子层里,然后由里往外依次排布在能量逐渐升高的电子层里。即先排布K层,当K层排满后,再排L层,等等。
以上四条规律是相互联系的,不能孤立地理解其中的一条,如M层不是最外层时,其容纳的电子数最多为18个,当其为最外层时,其容纳的电子数最多却为8个。
状元笔记:
原子最外层电子排满8个(当K层时排2个)时称为稳定结构,其他的电子层结构为不稳定结构。不稳定结构在一定条件下能变成稳定结构。
【示例】某原子第n电子层,当它作为最外层时,容纳电子数最多与n-1层相同,当它作为次外层时,其电子数比n-1层多10个,则此电子层是( )
A.K层
B.L层
C.M层
D.N层
解析:根据核外电子排布规律可知,核外电子分层排布,分别为K、L、M、N、O、P、Q……n值依次为1、2、3、4、5、6、7……每层最多可容纳电子2n2个,因此,L层n值为2,无论作为最外层还是次外层,最多都排布8个电子;而M层n值为3,当它作为最外层时只能排8个(与L层相同),若作为次外层,则可排18个,就比L层多10个电子。
答案:C
4.原子结构示意图
结构示意图包括原子结构示意图和离子结构示意图。结构示意图是用小圆圈和圆圈内的符号及数字表示原子核及核内质子数,弧线表示各电子层,弧线上的数字表示该电子层上的电子数。如:
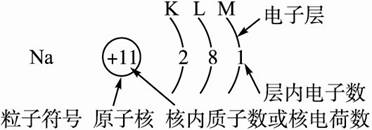
状元笔记:
原子结构示意图中,核内质子数等于核外电子数。
技术提示:离子结构示意图中,核内质子数与核外电子数不相等。如:
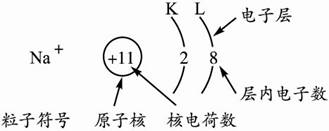
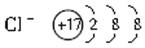
阳离子中,核电荷数大于核外电子数。阴离子中,核电荷数小于核外电子数。
【示例】下列粒子的结构示意图表示正确的是( )
A.18O的结构示意图: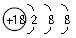
B.O2-的结构示意图: 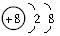
C.Mg2+的结构示意图: 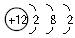
D.Mg2+的结构示意图: 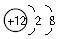
解析:18O的核电荷数为8,核外有8个电子,O2-的核电荷数为8,核外有10个电子;Mg失去最外层的两个电子后,次外层变成最外层。
答案:BD
二、核外电子排布对元素化学性质的影响
元素的化学性质活泼与否是由原子的最外层电子数决定的:
①稀有气体元素的原子最外层电子数为8个或2个,均为稳定结构,在化学反应中不易得到电子,也不易失去电子,所以化学性质比较稳定,一般不与其他物质发生化学反应;
②金属元素最外层电子数一般少于4个,在化学反应中容易失去最外层的电子,使最外层的电子数达到8个电子的稳定结构;
③非金属元素原子的最外层电子数大于或等于4个,在化学反应中容易得到电子,使最外层达到8个电子的稳定结构。
在上表所列举的原子中,碳、氧、硫、氯原子具有非金属原子的结构;钠、镁具有金属原子的结构;氖具有稀有气体原子的结构。
状元笔记:
在化学反应中,原子的核外电子可以得到或失去,但原子核不会改变。
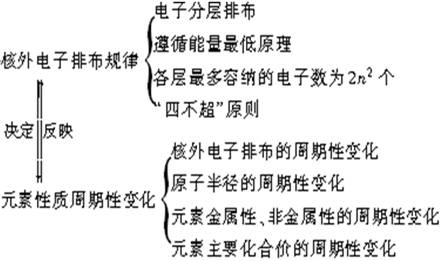
归纳整理
由于原子核外电子的排布规律:每隔一定数目的原子,最外层电子数出现周期性的变化,从而影响到元素的性质也出现周期性的变化。
思考发现
1~18号元素的原子结构的特殊性
(1)原子核中无中子的原子: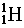 。
。
(2)最外层电子数与次外层电子数存在的倍数关系:
最外层电子数与次外层电子数相等的是Be、Ar;
最外层电子数是次外层电子数2倍的是C;
最外层电子数是次外层电子数3倍的是O;
最外层电子数是次外层电子数4倍的是Ne;
最外层电子数是次外层电子数1/2的是Li、Si。
(3)最外层电子数与其他电子层的关系:
电子层数与最外层电子数相等的原子有:H、Be、Al;
电子总数是最外层电子数2倍的原子有:Be;
内层电子数是最外层电子数2倍的原子有:Li、P。









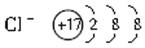
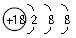
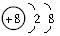
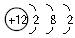
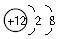

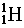 。
。